Mediante una técnica conocida como CRISPR, un grupo de investigadores de Oregon logró modificar el ADN de 42 embriones humanos. ¿A dónde conduce este camino, que hoy se inicia con la prevención de una enfermedad hereditaria del corazón?
24 de agosto de 2017
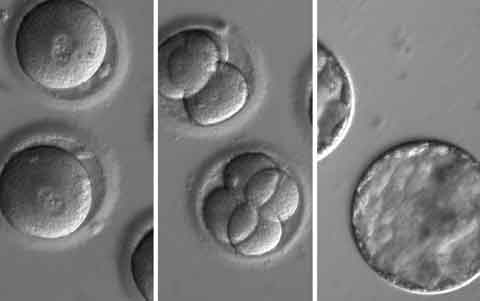
El anuncio vio la luz el último 2 de agosto en las páginas de las revista científica Nature: mediante una técnica de edición genética conocida como CRISPR, la cual permite «cortar» una porcioncita de genoma entre dos puntos predeterminados y reemplazarla por otra, se logró, por primera vez en la historia, «corregir» la anomalía genética causante de una enfermedad hereditaria del corazón (llamada miocardiopatía hipertrófica) en un embrión humano.
Los científicos autores del estudio –un equipo integrado por investigadores estadounidenses, chinos y coreanos liderado por el kazajo Shoukhrat Mitalipov, del Centro de Terapia Genética y Embriología Celular de la universidad OHSU de Oregon– aseguraron que la anomalía causante de la enfermedad pudo ser eliminada y reemplazada por una secuencia de ADN normalizada en un 72,4% de los embriones tratados, y que la técnica puede ser aplicada también en óvulos y espermatozoides.
Una alternativa posible es leer esta noticia como una novedad potencialmente auspiciosa para evitar en el futuro la transmisión de este tipo de cardiopatía, que afecta a una de cada 500 personas, genera un riesgo de muerte del 0,5% anual y, aunque no se cura, tiene tratamiento médico, según información que figura en la página web de la Sociedad Argentina de Cardiología (por otra parte, también es posible prevenirla mediante la técnica de diagnóstico genético preimplantatorio o PGD). Pero lo insoslayable y más inquietante es que, con el éxito de este experimento, virtualmente se abre la puerta de entrada al diseño de bebés mediante «cut and paste» de ADN. Al menos, en cuento a posibilidades técnicas.
La técnica CRISPR (que significa repeticiones palindrómicas cortas agrupadas y regularmente espaciadas) está inspirada en un mecanismo natural con que ciertos microorganismos defienden de los virus su material genético, y se emplea experimentalmente desde 2013, con ADN no solo humano. Es aparentemente sencilla: solo se requiere una cadena guía de ARN exactamente complementaria y con la misma longitud, como un «molde en negativo», del tramo de ADN que se quiere «editar», y dos moléculas de una proteína (Cas) para «cortar» los extremos.
Células vivas
En la práctica, explica la doctora en bioquímica Irene Szilan, investigadora en genética del CONICET, no es difícil hacerlo en un tubo de ensayo, aunque los reactivos y las cadenas de ARN con la calidad y la pureza necesarias son muy costosos. En Argentina hay proyectos de investigación con CRISPR. Lo que es mucho más difícil, asegura, es hacerlo en células vivas y, sobre todo, lograr exactamente los resultados deseados, porque los mecanismos por los cuales se repone en la célula el tramo de ADN editado «normal» son bastante complejos.
El futuro de la técnica de CRISPR, a la que la especialista definió como «muy auspiciosa para el tratamiento a futuro de muchas enfermedades genéticas», dependerá de que se perfeccionen y estandaricen procedimientos para editar cada gen específico. Las alrededor de 8.000 patologías genéticas hereditarias que se conocen serían las principales candidatas, especialmente las causadas por un solo gen. En las enfermedades más prevalentes a nivel de salud pública (como la hipertensión o la diabetes, por ejemplo) la influencia del factor genético es mucho más compleja e incluso indirecta, porque intervienen el ambiente y la historia de vida. Muchos rasgos físicos sí, dependen de los genes. Por eso, es la clase de innovaciones que implican una imprescindible discusión social, jurídica y política sobre los usos y los límites.
Los 42 embriones modificados en el experimento de Mitalipov fueron desechados; no habrá –todavía– bebés «editados» mediante CRISPR. Pero esto recién empieza.




